
Kandungan
Elektron valensi adalah elektron lapisan terluar yang boleh diisi oleh atom. Mereka adalah penting, kerana mereka biasanya terlibat dalam tindak balas kimia. Jadual berkala unsur adalah rujukan praktikal untuk menentukan dengan cepat bilangan elektron valensi dalam atom. Walau bagaimanapun, perlu diingatkan bahawa banyak elemen, kebanyakannya logam peralihan dan juga beberapa bukan logam, mungkin mempunyai beberapa keadaan valensi, bergantung kepada sebatian khusus.
Arahan
-
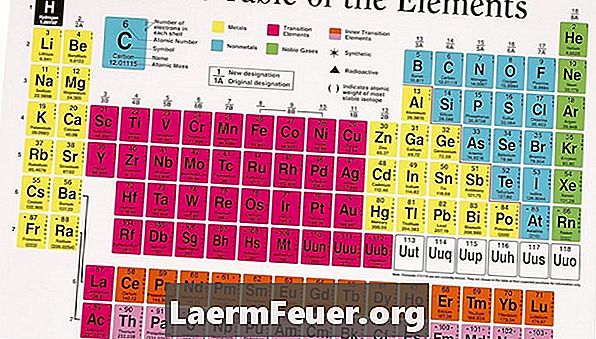
Cari elemen dalam jadual berkala. Mereka terletak di meja dengan nombor atom dari kiri ke kanan, atas ke bawah. Susunan unsur-unsur dalam baris sesuai dengan sifat-sifat yang dikongsi di antara mereka dalam suatu lajur yang diberikan, dengan ketara ditadbir oleh persamaan dalam susunan elektron-elektron ini.
-
Kenal pasti lajur di mana unsur berada. Setiap lajur dinamakan dengan nombor berhampiran bahagian atasnya. Sistem penomboran yang kini diterima oleh IUPAC secara berurutan berjumlah antara 1 hingga 8. Sebelum ini, IUPAC menamakan lajur 1A, 2A, 3A, dan sebagainya. Walaupun jadual berkala baru mesti ditukar kepada sistem baru, yang lama boleh menggunakan tatanama sebelumnya.
-
Mengira bilangan lajur dari kiri ke kanan, mengabaikan logam peralihan dan lajur terakhir di sebelah kanan. Tuliskannya sebagai bilangan elektron valensi. Sebagai contoh, menggunakan sistem penomboran sebelumnya, hanya menulis angka Roman dalam lajur yang dinamakan nombor elektron valensi, untuk elemen dalam kumpulan IA, IIA, IIIA, IVA, VA, VIA dan VIIA.
-
Tulis sifar untuk bilangan elektron valens untuk unsur-unsur kumpulan 18 (dahulunya dikenali sebagai kumpulan VIIIA). Unsur-unsur ini memperlihatkan lapisan elektron terluar diisi, dan umumnya tidak terlibat dalam tindak balas kimia.
-
Menulis perkataan "bervariasi" untuk unsur-unsur yang terletak di blok logam peralihan jadual berkala, kerana susunan elektron dalam unsur-unsur ini membolehkan mereka dalam lapisan terdalam untuk mengambil bahagian dalam tindak balas kimia. Ini menjadikan mereka kelihatan mempunyai valensi yang berubah dalam tindak balas yang berbeza. Besi, sebagai contoh, kadang-kadang bertindak balas dengan menggunakan dua elektron, dan tiga lagi, memberikannya satu valensi yang jelas dua atau tiga.
Apa yang anda perlukan
- Jadual Berkala Berkala